Asitler ve bazların hangi ortak özellikleri vardır?
Asitler ve bazlar, kimyanın temel bileşenleridir ve birçok ortak özellik taşırlar. Su ile etkileşimleri, pH değerleri, elektriksel iletkenlikleri, nötralizasyon tepkimeleri ve korozyon etkileri bu özellikler arasında yer alır. Bu özellikler, asitlerin ve bazların çeşitli uygulamalardaki önemini vurgular.
Asitler ve Bazların Ortak Özellikleri Asitler ve bazlar, kimyada önemli iki bileşen grubudur ve çeşitli özellikleri ile birbirlerinden ayrılmalarına rağmen, bazı ortak özelliklere de sahiptirler. Bu makalede, asitler ve bazların sahip olduğu ortak özellikler detaylı bir şekilde incelenecektir. 1. H2O ile Etkileşim Asitler ve bazlar, su ile etkileşime girdiklerinde belirli tepkimeler gösterirler. Asitler, su ile birleşerek hidrojen iyonları (H⁺) üretirken, bazlar ise hidroksit iyonları (OH⁻) üretir. Bu etkileşim, pH seviyesinin değişmesine ve çözeltilerin asidik veya bazik özellikler kazanmasına yol açar.
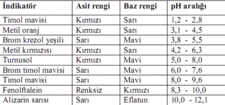
2. pH Değeri Asitler ve bazlar, pH değerleri ile tanımlanan özelliklere sahiptir. Asitlerin pH değeri genellikle 0-6 arasında bulunurken, bazların pH değeri 8-14 arasında yer alır. pH değeri, bir çözeltinin asidik veya bazik özelliklerini belirleyen önemli bir parametredir.
3. Elektriksel İletkenlik Asitler ve bazlar, su içinde çözündüklerinde elektriksel iletkenlik gösterirler. Bu özellik, çözeltideki iyonların varlığı ile ilgilidir. Asitler, H⁺ iyonları üretirken, bazlar OH⁻ iyonları üretir. Bu iyonlar, elektrik akımını iletebilir.
4. Nötralizasyon Tepkimesi Asitler ve bazlar, birbirleri ile nötralizasyon tepkimesi verirler. Bu tepkime, asit ve bazın birleşmesi sonucunda su ve bir tuz oluşur. Bu süreç, asit-baz kimyasında önemli bir yer tutar.
5. Korozyon Özelliği Asitler ve bazlar, birçok metal ve organik bileşenler üzerinde korozyon etkisi gösterirler. Bu özellik, asitlerin ve bazların reaktif doğasından kaynaklanmaktadır.
Sonuç Asitler ve bazlar, kimya alanında önemli iki bileşendir ve çeşitli ortak özelliklere sahiptirler. Bu özellikler, asitlerin ve bazların su ile etkileşimi, pH değerleri, elektriksel iletkenlik, nötralizasyon tepkimeleri ve korozyon etkileri gibi konuları kapsamaktadır. Bu iki grup bileşen, birçok endüstriyel ve bilimsel uygulamada kritik bir rol oynamaktadır. Ekstra Bilgiler Asitler ve bazlar, günlük yaşamda da sıkça karşılaşılan maddelerdir. Örneğin, limon suyu ve sirke asidik özellikler taşırken, sabun ve amonyak bazik özellikler taşır. Bu nedenle, asitler ve bazlar, hem kimya derslerinde hem de pratik hayatta önemli bir yer tutmaktadır. |








.webp)













.webp)
.webp)