
Potasyum kromat asidik mi yoksa bazik bir özellik mi taşır?
Potasyum kromat (K2CrO4), sarı renkli kristaller halinde bulunan önemli bir inorganik bileşiktir. Su ile etkileşimi asidik ve bazik özelliklerini belirler. Endüstride boyar maddeler ve analitik kimyada kullanımı yaygındır. Ancak, toksik etkileri nedeniyle güvenlik önlemleri gerektirir.
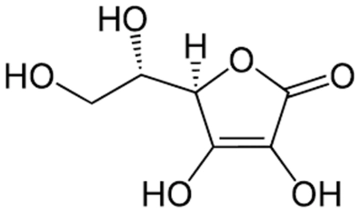
Potasyum kromat (K2CrO4), inorganik bir bileşiktir ve kimya alanında önemli bir yere sahiptir. Genellikle sarı renkli kristaller halinde bulunan bu bileşik, çeşitli endüstriyel uygulamalarda ve laboratuvar çalışmalarında kullanılır. Potasyum kromatın asidik veya bazik özellikleri, kimyasal yapısı ve su ile olan etkileşimleri göz önünde bulundurularak incelenebilir. Bu makalede, potasyum kromatın asidik veya bazik özellikleri detaylı bir şekilde ele alınacaktır. Potasyum Kromatın Kimyasal Yapısı Potasyum kromat, kromat iyonu (CrO4^2-) ve potasyum iyonu (K+) bileşenlerinden oluşur. Kromat iyonu, bir merkezi krom atomunun dört adet oksijen atomu ile çevrili olduğu tetrahedral bir yapıya sahiptir. Kromatın bu yapısı, onun asidik veya bazik davranışlarını belirleyen etmenlerden biridir. Kromat iyonunun yapısındaki oksijen atomları, su ile etkileşime girdiğinde proton (H+) alabilir veya verebilir. Asidik ve Bazik Özellikler Asidik ve bazik özellikler, bir maddenin su ile olan etkileşiminde belirginleşir. Bir madde asidik ise suya proton bırakma eğilimindedir, bazik ise proton alma eğilimindedir. Potasyum kromat, su içerisinde çözündüğünde aşağıdaki denklemi oluşturur: K2CrO4 (s) ⇌ 2 K+ (aq) + CrO4^2- (aq) Bu denkleme göre, kromat iyonu su ile etkileşime girdiğinde proton alma kapasitesine sahiptir. Ancak, potasyum kromat su içinde nötr bir pH değeri etrafında çözünür. Bununla birlikte, potasyum kromatın çözeltisi, özellikle asidik ortamlarda daha fazla reaktif hale gelir.
Potasyum Kromatın Kullanım Alanları Potasyum kromat, birçok endüstride yaygın olarak kullanılmaktadır. Bu kullanımlar arasında:
Sonuç Potasyum kromat, su ile etkileşime girdiğinde nötr pH değerine sahip bir bileşiktir. Ancak, asidik veya bazik ortamlarda farklı davranışlar sergileyebilir. Genel olarak, potasyum kromatın asidik veya bazik özellikleri, kimyasal yapısı ve su ile etkileşimleri göz önüne alındığında, asidik özellikler gösterme eğiliminde olduğu söylenebilir. Bununla birlikte, potasyum kromatın kullanıldığı alanlar ve uygulamalar, bu özelliğin önemini artırmaktadır. Ek Bilgiler Potasyum kromatın sağlık ve çevre üzerindeki etkileri de göz önünde bulundurulmalıdır. Krom bileşenleri genellikle toksik olarak kabul edilir. Bu nedenle, potasyum kromat ile çalışırken uygun güvenlik önlemleri alınmalı ve atık yönetimi kurallarına uyulmalıdır. Ayrıca, potasyum kromatın bazı kimyasal reaksiyonları sonucu, çevreye zararlı krom bileşenleri açığa çıkabilir. Bu durum, potasyum kromatın kullanımını sınırlayan önemli bir faktördür. Sonuç olarak, potasyum kromatın asidik ve bazik özellikleri, kimyasal yapısı ve çevresel etkileri bakımından detaylı bir inceleme gerektirmektedir. Bu incelemeler, potasyum kromatın endüstriyel kullanımları ve güvenlik önlemleri açısından daha iyi bir anlayış geliştirilmesine katkı sağlayacaktır. |








.webp)













.webp)
.webp)

Potasyum kromatın kimyasal yapısı ve asidik-bazik özellikleri hakkında daha fazla bilgi edinmek istiyorum. Özellikle kromat iyonunun su ile etkileşiminde proton alıp verme kapasitesinin nasıl işlediğini merak ediyorum. Bu durum, potasyum kromatın endüstriyel uygulamalarındaki kullanımını nasıl etkiliyor? Ayrıca, asidik ve bazik ortamlarda neden farklı davranışlar sergilediği konusunda daha fazla ayrıntı verir misin?
Bedih,
Potasyum Kromatın Kimyasal Yapısı
Potasyum kromat (K2CrO4), krom (Cr) ve kromat iyonu (CrO4^2-) içeren bir tuzdur. Yapısında potasyum (K) katyonları ve kromat anyonları bulunur. Kromat iyonu, merkezi krom atomunun dört oksijen atomu ile çevrili olduğu tetrahedral bir yapıya sahiptir. Bu yapı, kromatın asidik-bazik özelliklerini etkileyen önemli bir faktördür.
Asidik-Bazik Özellikler
Kromat iyonu, su ile etkileşime girdiğinde proton alıp verme kapasitesine sahiptir. Asidik ortamda, kromat iyonu (CrO4^2-) sülfürik asit (H2SO4) gibi asitlerle tepkimeye girerek dikromat iyonuna (Cr2O7^2-) dönüşebilir. Bu süreç, pH seviyesine bağlı olarak gerçekleşir. Yüksek pH'larda kromat iyonları baskınken, düşük pH'larda dikromat iyonları daha fazla görülür. Bu dönüşüm, potasyum kromatın asidik ve bazik ortamlarda farklı davranışlar sergilemesine yol açar.
Endüstriyel Uygulamalar
Potasyum kromat, özellikle pigment üretimi, metal kaplama ve su arıtma gibi birçok endüstriyel uygulamada kullanılır. Kromat iyonunun asidik ve bazik ortamlardaki davranışları, bu uygulamaların verimliliğini etkiler. Örneğin, metal kaplama işlemlerinde pH kontrolü, istenen kalitenin elde edilmesi için kritik öneme sahiptir.
Ayrıca, potasyum kromatın asidik ortamdaki dönüşümü, çevresel süreçler ve atık yönetimi açısından da önemlidir. Bu özellik, kromatın su arıtma sistemlerinde kullanımı sırasında dikkat edilmesi gereken bir faktördür.
Sonuç olarak, potasyum kromatın kimyasal yapısı ve proton alıp verme kapasitesi, endüstriyel uygulamalardaki verimliliği ve çevresel etkileri üzerinde önemli bir rol oynamaktadır.