
Asit ve Bazların Sulu Çözeltileri
Asitler ve bazlar, sulu çözeltilerinde çeşitli özellikler sergileyen kimyasal bileşenlerdir. Bu yazıda, asitlerin ve bazların sulu çözeltilerindeki davranışları, pH değerleri ve tepkimeleri gibi temel konular ele alınıyor. Ayrıca, günlük hayatta ve endüstrideki pratik uygulamaları da incelenmektedir.
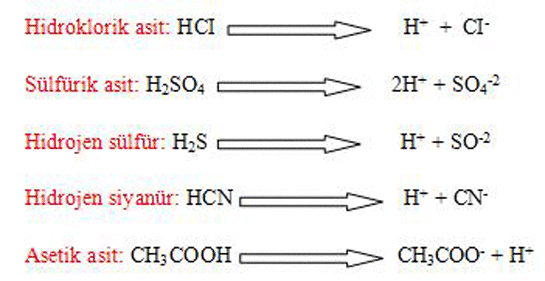
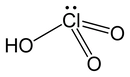
Asit Ve Bazların Sulu Çözeltileri Asitler ve bazlar, kimyada önemli birer bileşen olup, su ile etkileşimlerinde belirli özellikler gösterirler. Bu özellikler, asitlerin ve bazların doğası, davranışları ve çözünürlükleri ile doğrudan ilişkilidir. İşte asit ve bazların sulu çözeltilerinin detaylı bir incelemesi. 1. Asitlerin Sulu Çözeltileri Asitler, sulu çözeltilerinde proton (H⁺) veren maddeler olarak tanımlanır. Bu özellikleri, asitlerin su ile etkileşiminde belirgin bir şekilde ortaya çıkar. Asitlerin sulu çözeltileri aşağıdaki gibi çeşitli özellikler taşır:
2. Bazların Sulu Çözeltileri Bazlar, sulu çözeltilerinde hidroksit (OH⁻) iyonu veren maddelerdir. Bu özellikleri, bazların su ile etkileşiminde belirgin bir şekilde ortaya çıkar. Bazların sulu çözeltileri aşağıdaki gibi çeşitli özellikler taşır:
3. Asit-Baz Teorileri Asit ve bazların tanımlanması için çeşitli teoriler geliştirilmiştir. Bunlar arasında en yaygın olanları Arrhenius, Bronsted-Lowry ve Lewis teorileridir:
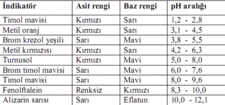
4. Sulu Çözeltilerde pH Değeri pH, bir çözeltinin asidik veya bazik özelliklerini belirlemek için kullanılan bir ölçek olup, 0 ile 14 arasında değer alır. pH değeri 7'den düşük olan çözeltiler asidik, 7'den yüksek olanlar ise bazik olarak kabul edilir. Bu bağlamda:
5. Asit-Baz Tepkimeleri Asitler ve bazlar arasında gerçekleşen tepkimelere asit-baz tepkimeleri denir. Bu tepkimeler, genellikle tuz ve su oluşumuyla sonuçlanır. Örneğin:
6. Pratik Uygulamaları Asitler ve bazlar, günlük yaşamda ve endüstriyel uygulamalarda birçok alanda kullanılmaktadır:
Sonuç olarak, asitler ve bazlar, sulu çözeltilerinde çeşitli özellikler gösteren önemli kimyasal bileşenlerdir. Bu özelliklerin anlaşılması, çok sayıda bilimsel ve pratik uygulama için kritik öneme sahiptir. Asit-baz kimyası, hem teorik hem de uygulamalı alanlarda derinlemesine bir bilgi birikimi gerektiren bir konudur. |








.webp)













.webp)
.webp)

Asitlerin sulu çözeltilerinde H+ iyonu vermesi ve elektrik iletkenliği göstermesi gerçekten de dikkat çekici bir durum. Ancak bu çözeltilerle çalışırken, güvenlik önlemlerinin ne kadar önemli olduğunu deneyimle anladım. Özellikle koruyucu kıyafetler giymek, asitlerin ciltle temasını önlemek açısından hayati bir önem taşıyor. Ayrıca, ortamın iyi havalandırılması gerektiğini de zamanla öğrendim. Çünkü bazı asitler su ile tepkimeye girdiğinde zararlı gazlar açığa çıkabiliyor. Bu nedenle, çalıştığım alanı düzenli olarak havalandırmak ve uygun ekipmanları kullanmak, hem sağlığım hem de güvenliğim için kritik hale geldi. Bu tür maddelerle çalışırken dikkatli olmak, ileride karşılaşabileceğim olumsuzlukları en aza indirmek açısından büyük bir fayda sağladı.
Asitlerle Çalışmanın Önemi
Dirayet, asitlerle çalışırken güvenlik önlemlerinin ne kadar kritik olduğunu vurgulaman çok önemli. Asitlerin sulu çözeltilerinin H+ iyonu vermesi ve elektrik iletkenliği göstermesi, bu maddeleri kullanırken dikkatli olmayı gerektiriyor.
Koruyucu Kıyafetlerin Önemi
Koruyucu kıyafetler giymek, ciltle temasın önlenmesi açısından hayati bir öneme sahip. Bu tür önlemler, olası kazaların etkilerini azaltmada büyük rol oynuyor.
Havalandırma ve Gazlar
Ayrıca, ortamın iyi havalandırılması gerektiğini belirtmen de çok yerinde. Bazı asitlerin su ile tepkimeye girmesi zararlı gazların ortaya çıkmasına neden olabilir. Bu yüzden çalıştığın alanı düzenli olarak havalandırmak, sağlığın ve güvenliğin için kritik bir adım.
Dikkatli Olmanın Faydası
Sonuç olarak, bu tür maddelerle çalışırken dikkatli olmak, gelecekte karşılaşabileceğin olumsuzlukları en aza indirmek için oldukça faydalı. Bilgini ve deneyimlerini paylaşman, diğerleri için de önemli bir farkındalık yaratıyor.
Asitlerin sulu çözeltilerinde H+ iyonu vererek elektrik iletkenliği göstermesi gerçekten ilginç. Ancak, bu tür çözeltilerle çalışırken nelere dikkat etmeliyim? Özellikle koruyucu kıyafetler ve ortam havalandırması konusunda daha fazla bilgi verebilir misiniz?
Elbette Onar, asitlerin sulu çözeltileri ile çalışırken dikkat etmeniz gereken birkaç önemli nokta vardır.
Koruyucu Kıyafetler:
Asitler tehlikeli kimyasallar oldukları için, ciltle temasından kaçınmak çok önemlidir. Bu nedenle, laboratuvar önlüğü, koruyucu eldivenler ve gözlük gibi kişisel koruyucu ekipman kullanmalısınız. Özellikle yoğun asitlerle çalışırken, kimyasal dirençli eldivenler tercih edilmelidir.
Ortam Havalandırması:
Asitlerin buharları solunum yollarına zarar verebilir. Bu nedenle, iyi havalandırılmış bir ortamda çalışmanız önemlidir. Eğer mümkünse, kimyasal davlumbaz altında çalışarak buharların hızlıca ortamdan uzaklaştırılmasını sağlayabilirsiniz.
Acil Durum Ekipmanları:
Her zaman yakınınızda bir göz yıkama istasyonu ve acil durum duşu bulunmalıdır. Asit sıçraması durumunda, derhal bu ekipmanları kullanarak etkilenen bölgeyi bol su ile yıkamalısınız.
Umarım bu bilgiler size yardımcı olur. Güvenli çalışmalar dilerim!