
Asit baz tepkimeleri her zaman ekzotermik mi olur?
Asit-baz tepkimeleri, kimyasal reaksiyonlarda önemli bir yere sahiptir ve enerji değişimlerini etkileyen faktörleri içerir. Ekzotermik ve endotermik özellikler gösteren bu tepkimeler, çevresel koşullara bağlı olarak farklılık gösterir. Kimya dışında birçok alanda da kritik rol oynamaktadır.
Asit Baz Tepkimeleri ve Enerji Değişimi Asit-baz tepkimeleri, kimya alanında önemli bir yere sahiptir. Bu tepkimeler, asitlerin ve bazların birbirleriyle etkileşime girerek yeni maddeler oluşturduğu kimyasal reaksiyonlardır. Tepkime sırasında enerji değişimleri meydana gelir. Ancak, bu enerji değişimlerinin her zaman ekzotermik (ısı veren) olup olmadığı sorusu, derinlemesine incelenmesi gereken bir konudur. Asit ve Baz Kavramları Asitler, su ile çözüldüğünde hidrojen iyonları (H⁺) veren maddelerdir. Bazlar ise hidrojen iyonları ile etkileşime girerek bu iyonları nötralize eden maddelerdir. Asit-baz tepkimeleri, genel olarak şu şekilde temsil edilebilir:
Ekzotermik Tepkimeler Ekzotermik tepkimelerde, tepkime sonucunda çevreye enerji (genellikle ısı) salınır. Bu tür tepkimelerde, ürünlerin enerji seviyesi reaktörlerin enerji seviyesinden daha düşüktür. Asit-baz tepkimeleri çoğunlukla ekzotermik olarak kabul edilir, çünkü su oluşumu ve iyonların birleşmesi sırasında enerji açığa çıkar. Özellikle güçlü asitlerin ve bazların tepkimeleri genellikle ekzotermik özellik gösterir. Endotermik Tepkimeler Bununla birlikte, bazı asit-baz tepkimeleri endotermik (ısı alan) özellik gösterebilir. Endotermik tepkimelerde, ürünlerin enerji seviyesi reaktörlerden daha yüksektir ve bu süreçte çevreden enerji alınır. Örneğin, amonyum nitratın su ile çözünmesi endotermik bir tepkimedir.
Bu tür tepkimelerde, çözünme sürecinde çevreden ısı çekilir ve bu nedenle çevrede soğuma hissedilir. Tepkime Koşulları ve Enerji Değişimi Asit-baz tepkimelerinin ekzotermik veya endotermik olma durumu, çeşitli faktörlere bağlıdır:
Bu faktörler, tepkimenin enerji değişimini etkileyebilir. Örneğin, zayıf asit ve bazların tepkimeleri, genellikle daha düşük enerji değişimleri gösterirken, güçlü asit ve bazlar arasında gerçekleşen tepkimeler daha belirgin ekzotermik özellikler sergileyebilir. Sonuç Sonuç olarak, asit-baz tepkimeleri her zaman ekzotermik değildir. Tepkimenin ekzotermik veya endotermik olma durumu, kullanılan asit ve bazların özelliklerine, tepkime koşullarına ve oluşan ürünlerin enerji seviyelerine bağlıdır. Bu nedenle, her bir tepkimenin özel koşullarının detaylı bir şekilde incelenmesi gerekmektedir. Ekstra Bilgiler Asit-baz tepkimeleri, sadece kimyada değil, biyoloji, çevre bilimi ve mühendislik gibi birçok alanda da önemli rol oynamaktadır. Örneğin, asit-baz tepkimeleri, besinlerin sindirilmesi, asidik yağmurun çevre üzerindeki etkisi ve endüstriyel süreçlerin optimizasyonu gibi konularda kritik öneme sahiptir. Ayrıca, bu tepkimelerin anlaşılması, pH kontrolü ve çeşitli kimyasal proseslerin yönetimi açısından da büyük bir önem taşımaktadır. |








.webp)













.webp)
.webp)

Asit-baz tepkimeleri üzerine yaptığın açıklamalar gerçekten ilginç. Ekzotermik ve endotermik tepkimelerin nasıl farklılık gösterdiği konusunu net bir şekilde ifade etmişsin. Özellikle amonyum nitratın su ile çözünmesi örneği dikkat çekici. Peki, bu tür tepkimelerin sadece laboratuvar ortamında mı geçerli olduğunu düşünüyorsun yoksa günlük yaşamda da karşılaştığımız örnekleri var mı? Ayrıca, zayıf asit ve bazların tepkimelerinin neden daha düşük enerji değişimleri gösterdiğini merak ediyorum. Bu konuda daha fazla bilgi verebilir misin?
Acarkan Bey, memnuniyetle açıklıyorum:
Günlük Yaşam Örnekleri:
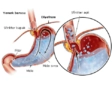
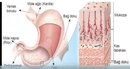
Asit-baz tepkimeleri günlük hayatımızın her alanında karşımıza çıkıyor. Mide asidinin antasit ilaçlarla nötralizasyonu, sirke (asetik asit) ile karbonatın (sodyum bikarbonat) temizlikte kullanılması, hatta sabunun yağları çözmesi hep asit-baz tepkimeleridir. Soğuk kompres paketlerinde amonyum nitrat benzeri endotermik tepkimeler kullanılırken, sıcak kompreslerde genellikle ekzotermik tepkimelerden yararlanılır.
Zayıf Asit-Baz Enerji Değişimleri:
Zayıf asit ve bazların düşük enerji değişimleri göstermesinin temel nedeni iyonlaşma derecelerinin düşük olmasıdır. Zayıf asitler suda kısmen iyonlaşır (örneğin asetik asit %1-2), bu nedenle tepkime sırasında kopan ve oluşan bağ sayısı daha azdır. Güçlü asit-baz tepkimelerinde tam iyonlaşma olduğu için daha fazla bağ kırılır ve oluşur, bu da daha yüksek enerji değişimine yol açar. Ayrıca zayıf asit-baz çiftleri genellikle daha kararlı yapılar oluşturduğundan enerji bariyeri daha düşüktür.