Bazı asit ve bazların kimyasal formülleri nelerdir?
Kimya bilimi, maddelerin yapısını ve değişimlerini incelerken asitler ve bazlar önemli bileşenlerdir. Bu yazıda, yaygın asit ve bazların kimyasal formülleri ve özellikleri ile kullanım alanları üzerinde durulmaktadır. Asitlerin ve bazların temel özellikleri, günlük yaşam ve endüstrideki rolleri açıklanacaktır.
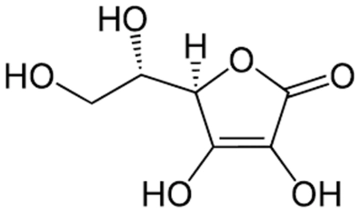
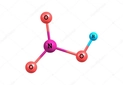
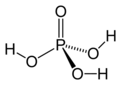
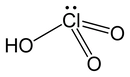
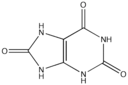
Kimya, madde ve onun değişimlerini inceleyen bir bilim dalıdır. Asitler ve bazlar, kimyasal reaksiyonlarda önemli rol oynayan bileşenlerdir. Bu makalede, bazı yaygın asit ve bazların kimyasal formülleri ile özellikleri ele alınacaktır. Asitler Asitler, sulu çözeltilerinde hidrojen iyonu (H⁺) salan maddelerdir. Asitlerin pH değeri 7'nin altındadır ve genellikle ekşi bir tatları vardır. İşte bazı yaygın asitler ve kimyasal formülleri:
Asitlerin Özellikleri Asitlerin temel özellikleri şunlardır:
Bazlar Bazlar, sulu çözeltilerinde hidroksit iyonu (OH⁻) salan maddelerdir. Bazların pH değeri 7'nin üzerindedir ve genellikle kaygan bir his verir. Bazı yaygın bazlar ve kimyasal formülleri şunlardır:
Bazların Özellikleri Bazların temel özellikleri şunlardır:
Asit ve Bazların Kullanım Alanları Asitler ve bazlar, çeşitli endüstriyel ve laboratuvar uygulamalarında yaygın olarak kullanılmaktadır:
Sonuç Asitler ve bazlar, kimya alanında temel bileşenler olup, birçok günlük yaşamda ve endüstride önemli roller oynamaktadır. Bu makalede, bazı yaygın asit ve bazların kimyasal formülleri ve özellikleri ele alınmış, ayrıca kullanım alanlarına değinilmiştir. Bu bilgilerin, asit ve bazların kimyasal özelliklerini anlamada yardımcı olacağı umulmaktadır. |








.webp)













.webp)
.webp)