
Asit Baz Tepkimeleri
Asit-baz tepkimeleri, kimyasal reaksiyonlar içinde önemli bir yer tutar. Bu yazıda, asit ve bazların tanımları, tepkimelerinin özellikleri, sınıflandırmaları ve uygulama alanları ele alınmaktadır. Asit-baz etkileşimlerinin günlük yaşam ve endüstrideki rolü vurgulanmaktadır.
Asit Baz Tepkimeleri Asit-baz tepkimeleri, kimyada asitlerin ve bazların birbirleriyle etkileşimi sonucu meydana gelen reaksiyonlardır. Bu tepkimeler, hem endüstriyel süreçlerde hem de biyolojik sistemlerde önemli bir rol oynamaktadır. Asitler, proton (H⁺) bağışlayıcıları olarak tanımlanırken, bazlar ise proton kabul edicileri olarak sınıflandırılır. Bu makalede asit-baz tepkimelerinin tanımı, özellikleri, sınıflandırılması ve uygulamaları üzerinde durulacaktır. Asit ve Baz Kavramları Asit ve bazların tanımı, farklı teorilere göre değişiklik göstermektedir. En yaygın kabul gören teoriler şunlardır:
Bu tanımlar, asit ve bazların kimyasal davranışlarını anlamamıza yardımcı olur. Asit Baz Tepkimelerinin Özellikleri Asit-baz tepkimeleri, bazı önemli özelliklere sahiptir:
Bu özellikler, asit-baz tepkimelerinin kimyasal süreçlerdeki önemini vurgulamaktadır. Asit Baz Tepkimelerinin Sınıflandırılması Asit-baz tepkimeleri çeşitli şekillerde sınıflandırılabilir:
Bu sınıflandırmalar, asit-baz tepkimelerinin çeşitli durumlarda nasıl gerçekleştiğini anlamamıza yardımcı olur. Asit Baz Tepkimelerinin Uygulamaları Asit-baz tepkimeleri, birçok alanda önemli uygulamalara sahiptir:
Bu uygulamalar, asit-baz tepkimelerinin günlük yaşamda ve endüstrideki önemini göstermektedir. Sonuç Asit-baz tepkimeleri, kimyasal reaksiyonların temel bir bileşenidir ve birçok alanda önemli rol oynamaktadır. Bu tepkimelerin anlaşılması, hem akademik hem de pratik alanlarda büyük bir öneme sahiptir. Gelecekteki araştırmalar, asit-baz tepkimelerinin daha derinlemesine incelenmesine ve yeni uygulama alanlarının keşfedilmesine olanak tanıyacaktır. Ek olarak, asit-baz tepkimelerinin çevresel etkileri, özellikle asidik yağmur ve su kirliliği gibi konular üzerinde daha fazla araştırma yapılması gerektiğini göstermektedir. Bu tür etkileşimlerin önlenmesi ve yönetilmesi, ekosistemlerin korunması açısından son derece önemlidir. |








.webp)













.webp)
.webp)

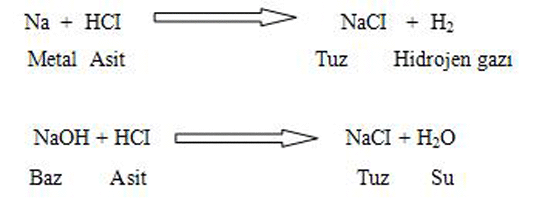
abi istedigim bu degil ki sadecsu tepkimesi tuz ile degil
Ferhat, merak etme, su tepkimesi tuz ile gerceklesmez. Su, genellikle asitler ve bazlarla tepkimeye girer. Tuzlar suyun icinde cozulerek iyonlarina ayrilir, ancak bu bir kimyasal tepkime degildir, fiziksel bir cozunmedir. Bu konuda daha fazla bilgi almak istersen, kimya ders kitaplarina goz atmani oneririm.
İstediğiniz şey bir asit veya bazın suyla tepkime vermesi ise size o tepkimeyi yazayım. Özellikle asit ve su tepkimeleri ekzotermik olduğu için dikkatli olunulmalıdır. Asit ve su tepkimeye girdiğinde etrafa sıçrama olamaması için dayanklı bir cam kapta yapılmalıdır. Asite su eklenmelidir.
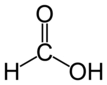
HCl + H2O Cl- + H3O+ oluşur.
Nurçin Küçükyılmaz denilen öğretmen müsveddesi dersi anlatmayıp bize konuları verip derste anlattırıyor ulan önce kendin anlat ta bizde anlatalım sonra saçma salak triplere girmesini iyi biliyor derste.
Anti Dünyalı, anladığım kadaryla Nurçin Küçükyılmaz'ın ders anlatma yöntemi seni rahatsız etmiş. Öğretmenlerin farklı öğretim metotları olabilir ve bazen bu metotlar öğrenciler tarafından beğenilmeyebilir. Bu durumu öğretmeninle yapıcı bir şekilde konuşarak onunla paylaşmanı tavsiye ederim. Belki bu şekilde bir çözüme ulaşabilirsiniz. Umuyorum ki dersleriniz daha verimli geçer.
Merhaba, anti dünyalı öncelikle kızgınlığını anlayabiliyorum fakat öğretmenler hayatımızın en güzel noktasında yer alıyorlar benimde ilk okulda sevmediğim bir öğretmenim vardı, sinir olduğum bir lafı vardı ama büyüdüğümde ben öğretmenimin o lafını hayatıma geçirdim ve çok faydasını gördüm şimdi sadece arkasından allah razı olsun diyorum ilerde sende öyle diyeceksin belkide..