
Asit ve bazların ph değerleri nasıl belirlenir?
pH, bir çözeltinin asidik veya bazik özelliklerini belirleyen önemli bir ölçüm birimidir. Bu içerikte, pH değerinin nasıl belirlendiği ve bu işlemlerde kullanılan yöntemler detaylı bir şekilde açıklanmaktadır. Asit ve bazların pH değerlerinin önemi de vurgulanmaktadır.
Asit ve Bazların pH Değerleri Nasıl Belirlenir?pH, bir çözeltinin asidik veya bazik (alkalik) özelliklerini belirlemek için kullanılan bir ölçü birimidir. 0 ile 14 arasında bir değere sahip olan pH ölçeği, 7 değerini nötr olarak kabul eder. Bu bağlamda, pH değeri 7'den düşük olan çözeltiler asidik, 7'den yüksek olanlar ise bazik olarak tanımlanır. pH değeri, bir çözeltideki hidrojen iyonu (H⁺) konsantrasyonunu gösterir. Bu yazıda, asit ve bazların pH değerlerinin belirlenmesi yöntemleri ayrıntılı bir şekilde ele alınacaktır. pH Ölçeğinin Temel İlkeleri pH, negatif logaritmik bir ölçü birimidir ve şu formülle tanımlanır: pH Değerinin Belirlenmesi Yöntemleri Asit ve bazların pH değerlerini belirlemenin birkaç farklı yöntemi bulunmaktadır:
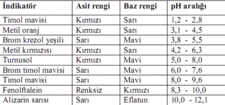
pH Metre Kullanımı pH metre, bir çözeltinin pH değerini hassas bir şekilde ölçmek için kullanılan bir cihazdır. pH metre ile ölçüm yapmak için öncelikle cihazın elektrotları, çözeltinin içine daldırılır. Cihaz, hidrojen iyonlarının konsantrasyonunu ölçerek pH değerini gösterir. Bu yöntem, özellikle laboratuvar ortamında yaygın olarak kullanılmakta olup, oldukça doğru sonuçlar verir. pH Kağıdı ile Test pH kağıdı, özel olarak hazırlanmış bir indikatör kağıdıdır. Bu kağıt, çözeltiye daldırıldığında renk değiştirir ve bu renk, pH değerini gösterir. pH kağıtları genellikle 1 ile 14 arasında farklı renk tonlarıyla kodlanmıştır. Kullanım kolaylığı ve pratikliği nedeniyle, özellikle saha uygulamalarında tercih edilmektedir. İndikatörler Kullanarak pH Belirleme Kimyasal indikatörler, pH değişimlerini tespit etmek için kullanılan bileşenlerdir. Örneğin, fenolftalein ve metil portakal gibi indikatörler, belirli pH aralıklarında renk değiştirir. Bu indikatörler, titrasyon gibi deneylerde sıklıkla kullanılır. Kimyasal Reaksiyonlar ile pH Hesaplama Asit ve bazların nötralizasyon reaksiyonları ile pH değeri hesaplanabilir. Bu yöntem, asit ve bazın bir araya getirilmesiyle oluşan tuz ve suyun pH değerinin belirlenmesini içerir. Örneğin, hidroklorik asit (HCl) ve sodyum hidroksit (NaOH) reaksiyona girdiğinde su ve sodyum klorür (NaCl) meydana gelir. Bu türreaksiyonların sonucunda oluşan çözeltinin pH değeri, başlangıçtaki asit ve bazların konsantrasyonlarına bağlı olarak hesaplanabilir. pH Değerinin Önemi pH değeri, birçok kimyasal ve biyolojik süreçte kritik bir rol oynamaktadır. Su kaynaklarının kalitesi, tarımda bitki büyümesi, gıda üretimi ve sağlık alanında birçok uygulamada pH değerinin izlenmesi önemlidir. Örneğin, tarımda toprak pH'ı, bitkilerin besin maddelerini ne kadar iyi alabileceğini etkileyebilir. Ayrıca, suyun pH değeri, sucul canlıların yaşama koşullarını belirler. Sonuç Asit ve bazların pH değerlerini belirlemek, hem laboratuvar hem de endüstriyel uygulamalarda önemli bir süreçtir. pH ölçüm yöntemleri, çözeltilerin asidik veya bazik özelliklerini değerlendirmek için farklı seçenekler sunmaktadır. Bu bilgiler, kimya, biyoloji, çevre bilimleri gibi birçok alanda kritik öneme sahiptir. pH değerinin doğru bir şekilde belirlenmesi, bu alanlarda gerçekleştirilen araştırmalarda ve uygulamalarda başarı için gereklidir. |








.webp)













.webp)
.webp)

pH değerlerinin belirlenmesi konusunda birçok yöntem olduğunu öğrenmek oldukça ilginç. Özellikle pH metre kullanımı, hassas ölçümler için pratik bir çözüm sunuyor. Sizce pH kağıdıyla yapılan testlerin sahada ne kadar güvenilir olduğunu söyleyebilir misiniz? Ayrıca, kimyasal reaksiyonlar ile pH hesaplama yöntemi, pratikte ne kadar sık kullanılıyor? Bu konuda deneyimlerinizi paylaşabilir misiniz?
Egesel bey, sorularınız pH ölçüm yöntemlerinin pratikteki kullanımına dair önemli noktalara değiniyor. Deneyimlerime dayanarak şunları paylaşabilirim:
pH Kağıdının Sahada Güvenilirliği
pH kağıtları, hızlı ve ekonomik olmaları nedeniyle saha çalışmalarında yaygın kullanılır. Ancak güvenilirlikleri bazı faktörlere bağlıdır:
- Kalibrasyon: Düşük kaliteli kağıtlar ±0.5-1 pH birimi hata payına sahip olabilir
- Renk yorumlama: Gözle renk karşılaştırması subjektif olabilir, özellikle ara tonlarda
- Ortam koşulları: Yüksek iyonik kuvvet veya yüksek sıcaklık ölçümü etkileyebilir
- Renkli veya bulanık çözeltilerde okuma zorlaşır
Sahada, acil durum değerlendirmeleri veya yaklaşık değer gerektiren durumlarda pH kağıtları yeterlidir, ancak hassas ölçümler için pH metre tercih edilmelidir.
Kimyasal Reaksiyonla pH Hesaplama
Bu yöntem genellikle laboratuvar ortamında ve eğitim amaçlı kullanılır:
- Pratik uygulamada, özellikle endüstriyel süreçlerde, direkt ölçüm yöntemleri daha yaygın
- Asit-baz titrasyonu ile pH hesaplama, daha çok analitik kimya laboratuvarlarında konsantrasyon belirleme için kullanılıyor
- Reaksiyon stokiyometrisi ve denge hesaplamaları, proses tasarımı veya teorik çalışmalarda önem taşıyor
Günlük pratikte, çoğu uygulama alanında (su arıtma, gıda, ilaç, tarım) direkt ölçüm cihazları tercih ediliyor. Kimyasal hesaplamalar daha çok araştırma, kalibrasyon veya proses validasyonu aşamalarında önem kazanıyor.
Her yöntemin kendi uygulama alanı bulunuyor - seçim, ihtiyaç duyulan hassasiyet, zaman, maliyet ve çalışma koşullarına göre değişiyor.