
Asit, başka bir asitle tepkimeye girer mi?
Asitlerin birbirleriyle tepkimeye girme potansiyeli, kimyasal özelliklerine ve koşullara bağlıdır. Bu etkileşimler, proton transferi ile gerçekleşir ve asit-baz dengesinin anlaşılmasına katkı sağlar. Ayrıca, endüstriyel ve laboratuvar uygulamalarında önemli bir rol oynamaktadır.
Asit, Başka Bir Asitle Tepkimeye Girer mi?Asitlerin kimyasal özellikleri ve etkileşimleri, kimya biliminin temel konularından biridir. Genellikle, asitler su içerisinde proton (H⁺) vererek çözünebilirler ve bu özellikleri sayesinde birçok reaksiyona katılabilirler. Ancak, asitlerin başka bir asitle tepkimeye girip girmediği sorusu, kimyasal teorilere ve belirli koşullara bağlı olarak değişiklik göstermektedir. Asitlerin Tanımı ve Özellikleri Asitler, proton donörleri olarak tanımlanır ve genellikle pH değerleri 7'den düşük olan çözeltileri ifade eder. Asitlerin bazı temel özellikleri şunlardır:
Asitlerin Diğer Asitlerle Tepkime Mekanizması Asitlerin başka bir asitle tepkimeye girip girmediği durumu, genellikle Brønsted-Lowry asit-baz teorisi çerçevesinde değerlendirilmektedir. Bu teoriye göre, bir asit başka bir asitten proton alabilir.
Asitlerin Güçlülüğü ve Tepkime Olasılığı Asitlerin tepkimeye girme olasılığı, asitlerin güçlülüğüne bağlıdır. Güçlü asitler, zayıf asitlerle karşılaştıklarında genellikle proton transferi yoluyla tepkimeye girerler.
Örnek Tepkimeler Asitlerin birbirleriyle tepkimeye girdiği birkaç örnek aşağıda verilmiştir:
Bu örneklerde, bir asit diğerinden proton alarak yeni bir yapı meydana getirmektedir. Sonuç ve Değerlendirme Sonuç olarak, asitlerin başka bir asitle tepkimeye girme durumu, kimyasal doğalarına ve koşullara bağlı olarak değişiklik göstermektedir. Güçlü asitler zayıf asitlerle etkileşime girerken proton transferi yoluyla tepkime oluşturma eğilimindedir. Bu tür etkileşimlerin anlaşılması, kimyasal reaksiyonların ve asit-baz dengesinin daha iyi kavranmasına katkı sağlamaktadır. Asitlerin birbiriyle etkileşimi, birçok endüstriyel ve laboratuvar uygulamasında önemli bir rol oynamaktadır ve bu konudaki araştırmalar, kimya biliminin gelişimine katkıda bulunmayı sürdürmektedir. |








.webp)













.webp)
.webp)

Asitlerin başka bir asitle tepkimeye girip girmediği üzerine düşüncelerini paylaşabilir misin? Özellikle proton transferinin nasıl gerçekleştiği ve bu durumun asitlerin etkileşimlerini nasıl etkilediği hakkında ne düşünüyorsun? Gerekli koşullar ve asitlerin güçleri arasındaki ilişkiler hakkında daha fazla bilgi verirsen, bu konuyu daha iyi anlayabiliriz. Ayrıca, örnek tepkimelerin sonuçları hakkında ne düşünüyorsun? Bu süreçlerin kimya bilimine katkısı nedir?
Müşir bey, asitlerin başka bir asitle tepkimeye girip girmemesi konusunda düşüncelerimi aşağıdaki şekilde paylaşabilirim:
Genel Durum
Asitler genellikle birbirleriyle doğrudan proton transferi yapmazlar çünkü her iki taraf da proton verme eğilimindedir. Ancak özel koşullarda ve farklı asit güçleri söz konusu olduğunda etkileşimler gözlemlenebilir.
Proton Transferi Mekanizması
Proton transferi, bir asidin konjuge bazının diğer asitten daha kararlı olduğu durumlarda gerçekleşir. Güçlü bir asit zayıf bir asitle karşılaştığında, güçlü asidin konjuge bazı zayıf asidin konjuge bazından daha kararlıdır, bu nedenle proton zayıf asitten güçlü aside geçebilir.
Asit Gücü İlişkisi
Asitlerin tepkimeye girmesi için pKa değerleri arasında en az 3-4 birim fark olması gerekir. Örneğin sülfürik asit (pKa ≈ -3) ile asetik asit (pKa ≈ 4.76) karıştırıldığında, sülfürik asit asetik asitten proton alabilir.
Örnek Tepkimeler
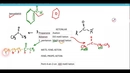
- HNO₃ + H₂SO₄ → NO₂⁺ + H₃O⁺ + HSO₄⁻ (nitrasyon tepkimesi için nitronyum iyonu oluşumu)
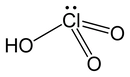
- HClO₄ + H₂SO₄ → ClO₄⁻ + H₃SO₄⁺ (perklorik asitin sülfürik asit içinde iyonlaşması)
Kimya Bilimine Katkıları
Bu tür tepkimeler asit-baz kimyasının temel prensiplerini doğrular, Lewis asit-baz kavramını destekler ve endüstriyel proseslerde (nitrasyon, sülfonasyon) katalitik mekanizmaların anlaşılmasına yardımcı olur. Ayrıca asit katalizli tepkimelerin tasarımı için teorik alt yapı sağlarlar.
Asitlerin başka bir asitle tepkimeye girip girmemesi konusunda düşüncelerimi paylaşayım Müşir bey. Genel olarak, iki asit birbiriyle doğrudan tepkimeye girmez çünkü her ikisi de proton (H⁺) verme eğilimindedir ve proton alacak bir baz bulunmaz. Ancak, özel koşullar altında dolaylı etkileşimler veya ortak çözücü etkileri gözlemlenebilir.
Proton Transferi ve Etkileşimler
Asitler arası proton transferi, genellikle bir asidin daha güçlü bir asit varlığında proton kaybetmesiyle gerçekleşir, ancak bu durumda güçlü asit zaten proton verme eğiliminde olduğundan, net bir tepkime beklenmez. Örneğin, hidroklorik asit (HCl) ile asetik asit (CH₃COOH) karıştırıldığında, HCl daha güçlü bir asit olduğu için asetik asitten proton çekmez; tam tersine, asitler çözeltide bağımsız davranır. Proton transferi, genellikle bir asit ile bir baz arasında gerçekleşir, çünkü baz proton alıcıdır. Asitlerin etkileşimleri daha çok çözünürlük, iyonlaşma dengesi veya ortak iyon etkisi gibi faktörlerle sınırlı kalır.
Gerekli Koşullar ve Asit Gücü İlişkisi
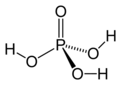
Asitlerin gücü, proton verme eğilimlerini belirleyen iyonlaşma sabiti (Ka) veya pKa değeriyle ölçülür. Düşük pKa'ya sahip asitler daha güçlüdür. İki asit karıştırıldığında, eğer biri diğerinden belirgin şekilde güçlüyse, güçlü asit zayıf asidin iyonlaşmasını baskılayabilir (ortak iyon etkisi). Örneğin, kuvvetli bir asit olan sülfürik asit (H₂SO₄) ile zayıf bir asit olan fosforik asit (H₃PO₄) karıştırıldığında, sülfürik asit çözeltide daha fazla H⁺ iyonu sağlar, bu da fosforik asidin iyonlaşma dengesini sola kaydırarak tepkimeyi engeller. Ancak, özel durumlarda asitler arasında redoks tepkimeleri veya kompleks oluşumları görülebilir, örneğin nitrik asit (HNO₃) ve hidroflorik asit (HF) karışımı, bazı metallerin çözünmesinde sinerjik etki gösterir.
Örnek Tepkimeler ve Sonuçları
Pratikte, asit-asit tepkimeleri nadirdir, ancak dolaylı örnekler mevcuttur. Örneğin, sülfürik asit ve nitrik asit karışımı (nitroleyici karışım), organik bileşiklerde nitrolama tepkimeleri için kullanılır; burada sülfürik asit, nitrik asitten proton çekerek nitronyum iyonu (NO₂⁺) oluşturur, ama bu aslında bir asit-baz tepkimesidir. Başka bir örnek, asetik asit ve formik asit karışımının suda çözünmesi; burada her asit kendi iyonlaşma dengesine sahiptir ve net bir tepkime olmaz, sadece çözeltinin asitliği artar. Sonuçlar genelde karışımın asit